科学家从肠道中发现,一种细菌能分解永久有毒的化学物质
你知道吗?你每天使用的不粘锅、防水衣、外卖盒,甚至化妆品中,都可能含有全氟和多氟烷基物质(PFAS),它们被称为“永远化学品”,几乎不会在自然环境中分解,能够在水、土壤、食物链乃至我们体内长时间存留。
更令人担忧的是,PFAS不仅污染环境,还悄然渗透到我们的身体深处,并可能带来多种健康风险。不过,最新一项发表于《自然微生物》(Nature Microbiology)的研究带来了一线希望。研究人员发现,我们体内的肠道细菌,竟然具备吸收和锁住PFAS的能力,还能帮助将其通过粪便排出体外。
肠道细菌也能“吃掉”永远化学品
长久以来,科学家们一直在寻找PFAS的解毒方法,最近由剑桥大学科研团队主导的研究,系统筛查了来自人类肠道的89种微生物,其中包括66种常见共生细菌和多种益生菌株。他们发现,有38种细菌能在不同浓度下高效吸附并积累PFAS,表现最突出的包括名为单形拟杆菌(Bacteroides uniformis)、内脏臭气杆菌(Odoribacter splanchnicus)等厌氧菌。
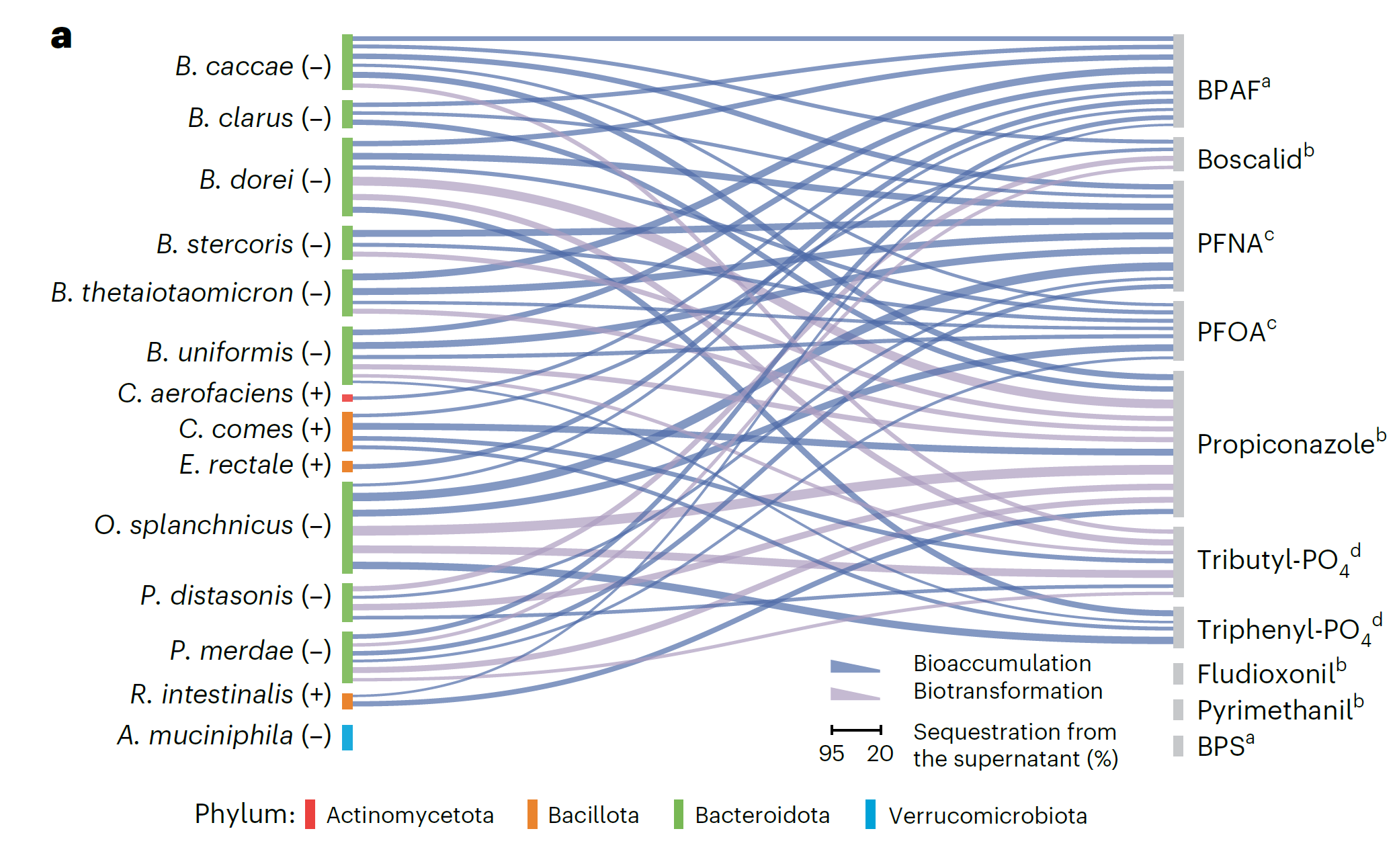
体肠道菌种能够在较宽浓度范围内富集并耐受PFAS(图片来源:参考文献[1])
上图利用质谱分析技术识别了人类肠道细菌在24小时生长周期内对化学污染物的富集和转化特异性。图中细菌种类与污染物之间的连线表示该细菌对该化合物的消耗率超过20%。
研究团队选择了两种典型的PFAS,全氟辛酸(PFOA)和全氟壬酸(PFNA)进行实验,结果显示O. splanchnicus厌氧菌在24小时内可吸收74%的PFNA 和 58% 的PFOA,而B. uniformis 厌氧菌也展现出稳定的吸附能力,并且在接触PFAS浓度高达500微摩尔,这样远高于自然暴露水平时,仍能正常生长,说明这些细菌对PFAS有一定耐受性。
这些结果令人惊讶,因为过去人们普遍认为PFAS这种表面活性物质只会黏附在细菌表面,难以进入细胞内部。而最新研究通过冷冻聚焦离子束质谱成像(FIB-SIMS)技术,首次清晰地看见PFAS实际聚集在细菌细胞内,并形成颗粒状团块。这不仅直接证实了PFAS能进入细胞,还表明细菌可能通过某种机制打包这些有毒物质,从而降低其对自身代谢的干扰。
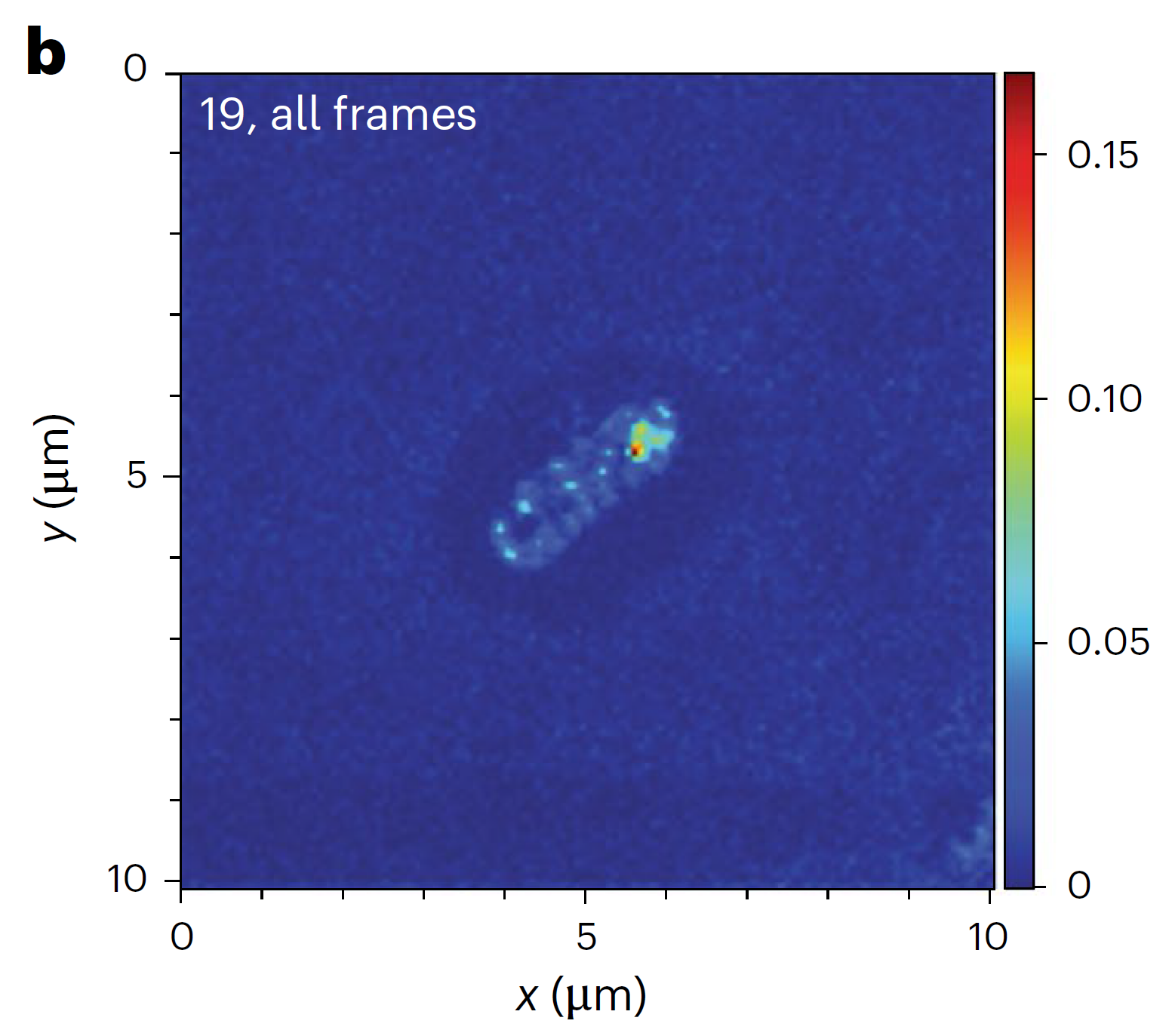
氟元素在细胞内部的分布(图片来源:参考文献[1])
更重要的是,在小鼠实验中,研究人员将9种高吸附能力的肠道细菌植入无菌小鼠肠道,并喂食PFNA。结果显示,相较于未接种细菌的小鼠,这些植入过细菌的老鼠在粪便中排出的PFAS显著增加,说明这些细菌确实在真实生理环境中也能帮助清理PFAS。
换句话说,我们的肠道菌群,可能不仅是消化食物的助手,还可能是处理有毒污染物的高手。
细菌靠什么“吃下”PFAS?
PFAS这类分子结构极其稳定,由强碳—氟键构成,表面同时拥有疏水链与亲水区域,既能穿透细胞膜,又可能干扰正常代谢。更何况,它们还有强烈的表面活性,与细胞膜脂质高度亲和,因此早期的观点普遍认为PFAS只能附着在细菌外膜上,而不是进入细胞内部。
那么,PFAS是如何进入细胞内部的呢?研究者指出,这一过程并非完全依赖被动扩散,而可能涉及特定的跨膜运输机制。在模型细菌大肠杆菌中,研究人员发现,如果去除一种多药排出泵的通道部分,也就是TolC外排蛋白,细胞内PFAS的积累量显著上升。这表明,细菌可能本身具备一定排毒机制,而TolC正是关键一环,当TolC缺失时,细菌就无法有效将PFAS排出,因而出现更高的胞内浓度。
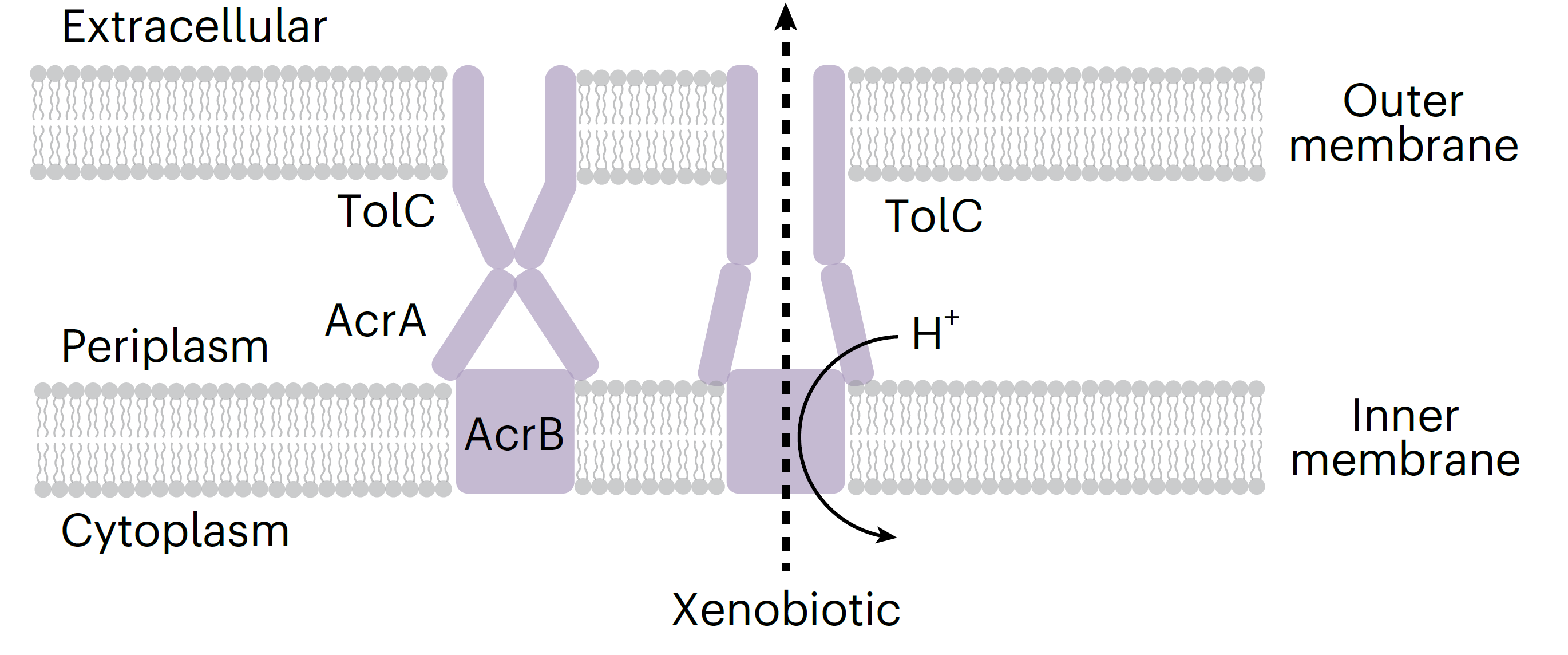
TolC外排泵示意图,图中左侧显示该泵处于静息状态;右侧则为其构象发生改变以将外源性化合物排出细胞的状态(图片来源:参考文献[1])
进一步的蛋白质组和代谢组分析也揭示了PFAS影响下的细胞反应。例如,在高吸附能力的B. uniformis厌氧菌中,研究者观察到多种膜相关蛋白表达上调,同时谷氨酸、天冬氨酸、色氨酸代谢通路出现变化。这说明细菌为应对胞内PFAS可能会启动一套适应策略,调节膜结构、代谢平衡以维持稳定状态。
这套机制的本质似乎并非摄入,而是一种偶发的物理—生物过程,由于PFAS的表面活性结构,它们可能自发聚集并与细胞质成分形成非共价结合体,一旦进入细胞,还可能通过与蛋白质或大分子相互作用形成聚集体,从而降低毒性。
能否制备排毒益生菌?
如果我们的肠道细菌真的能吃掉PFAS,是不是意味着只要补充点特殊的的益生菌,就能清理身体里的有毒化学物?这个想法听起来很诱人,但从科学角度来看,实现它并不容易。
这项研究虽然结果令人振奋,但目前仍然停留在小鼠实验阶段。肠道细菌确实有能力帮助清除部分PFAS,但实验有几个限制。暴露方式为一次性高剂量摄入,而人类现实中面临的是长期低剂量的慢性暴露,小鼠肠道菌群单一可控,而人类肠道环境复杂多变,菌群之间竞争、协同和稳定性都会影响功能菌的定殖和作用。未评估长期健康效益与副作用,比如是否影响其他代谢通路,是否会打破原有微生态平衡等。
除此之外,即便在实验中有些厌氧菌表现优异,在工业生产和口服益生菌制剂开发上也存在技术难题。它们通常对氧气极为敏感,需要特殊的封装和运输技术才能确保其在肠道中顺利着陆并长期存活。
此外,还有一个重要问题不容忽视,益生菌能吸收PFAS,却无法降解它们。也就是说,它们只是临时仓库,将PFAS聚集并送出体外,但并没有真正破坏这些分子的结构。排出的PFAS仍将回到环境中,如果处理不当,可能只是换了个地方藏。
总结
在与永远化学品的博弈中,剑桥大学等机构的研究显示,某些人类肠道细菌具备惊人的PFAS吸收能力,甚至能够帮助将其排出体外。
这一发现为首次揭示了人类肠道中的部分细菌具有强大的永远化学品生物富集能力,能够在细胞内“捕获”并固定这类有毒物质,并在动物模型中促进其排出体外。它不仅拓展了我们对肠道菌群功能的认知,还为未来开发基于益生菌的体内解毒手段提供了新的科学依据,尤其在面对难以避免的PFAS暴露背景下,提出了一种潜在的体内缓解新路径。
参考文献:
[1] Lindell, Anna E., et al. "Human gut bacteria bioaccumulate per-and polyfluoroalkyl substances." Nature Microbiology 10.7 (2025): 1-18.
[2] Cousins, Ian T., et al. "Outside the safe operating space of a new planetary boundary for per-and polyfluoroalkyl substances (PFAS)." Environmental Science & Technology 56.16 (2022): 11172-11179.
[3] Fan, Yong, and Oluf Pedersen. "Gut microbiota in human metabolic health and disease." Nature Reviews Microbiology 19.1 (2021): 55-71.
[4] Glüge, Juliane, et al. "An overview of the uses of per-and polyfluoroalkyl substances (PFAS)." Environmental Science: Processes & Impacts 22.12 (2020): 2345-2373.
作者丨杨超博士 中国科普作家协会会员
审核丨赵宝锋博士 辽宁生命科学学会
图文简介
