基因疗法只需注射一次,即可在数周内恢复聋哑患者的听力
有些孩子从一出生起,就生活在无声的世界。他们看得见嘴唇的开合,却听不见声音。对于这些因基因突变导致先天性耳聋的患者而言,听见声音变成了一种奢望。但如今,科学正在为他们打开一道新门——通过一次精确的基因注射,唤醒耳蜗深处沉睡的神经传导功能,让声音重新被接通。

基因疗法治疗失聪示意图(图片来源:作者使用AI生成)
人们为什么会失聪?
我们习以为常的听觉,其实每一个声音,从车鸣到鸟叫,首先被外耳收集,经中耳传入内耳中的耳蜗,在那里被转化为神经信号,最终传送至大脑进行解读。这套系统中的每一环节,都需要精密合作。而一旦任何一个“零件”出错,就可能导致我们再也听不到这个世界的声音。
在医学上,有一种特殊的听力障碍被称为“听觉神经病变”,它不是因为耳蜗的毛细胞坏了,而是因为耳蜗和听觉神经之间的信号传输出问题了。就像电报线还在、收发器也在,可信息偏偏就是无法送达。
在这类患者中,有一类遗传突变尤其关键——OTOF基因突变。这个基因编码一种叫做Otoferlin的蛋白,它专门负责在内耳的突触处“打包”并释放神经递质,把声音信号从耳蜗内的感觉毛细胞传递到听觉神经。想象一下,这是一个快递员,如果他缺席,声音信号快递就永远传不到大脑。研究显示,OTOF突变是导致先天性重度耳聋(DFNB9)的常见原因之一。
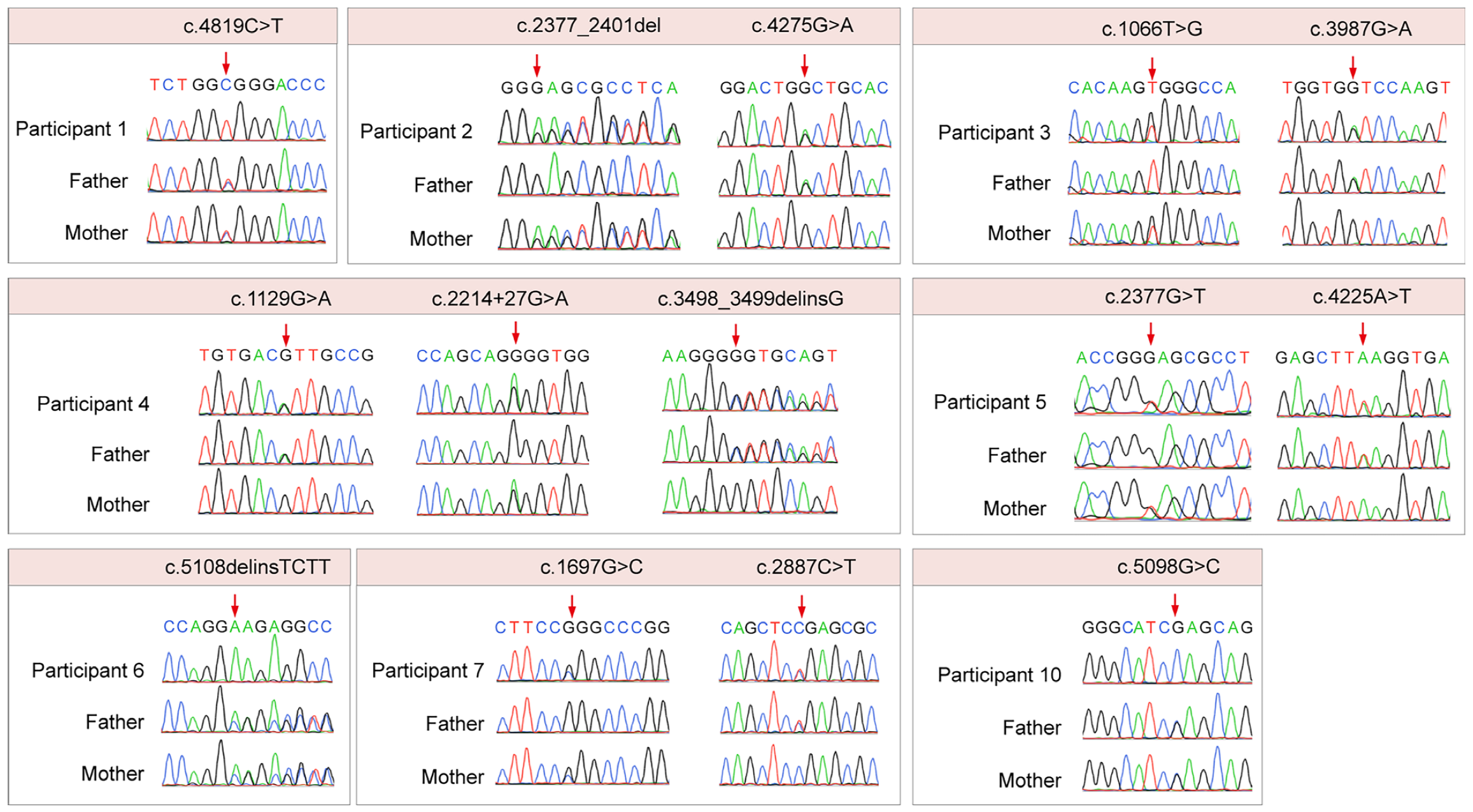
箭头标示OTOF等位基因中的变异(图片来源:参考文献[1])
一次注射,六个月改变人生:基因疗法如何工作?
想象一下,如果只需一次注射,就能让一个听不见世界的孩子开始听歌、说话,这是一件多么美好神奇的事情。在2025年春天,这样的故事在中国的五家医院中真实上演了。
这项由中国科研团队牵头发表于《自然医学》(Nature Medicine)的研究,尝试用一种名为AAV-OTOF基因疗法的方式,来修复由OTOF基因突变导致的先天性耳聋。他们招募了10位受试者,年龄从1.5岁到23.9岁不等,全部患有严重到极重度的听力障碍。治疗的核心思想其实并不复杂。既然原本的耳神经传导基因出错了,我们就补充一个正常的拷贝进去。
科学家们使用一种合成的腺相关病毒(AAV),将健康的OTOF基因包裹起来,然后通过耳后的微创手术,将其注射到耳蜗底部的“圆窗膜”处。这种注射位置看似简单,却是精准的神经接口,病毒进入耳蜗后,被毛细胞吸收,并在其中表达出正常的Otoferlin蛋白,从而恢复声音信号的接力传输。
最令人惊讶的是,这项治疗的起效速度之快、效果之显著。研究显示,平均听力阈值从106分贝提升至52分贝,大部分受试者在一个月内就开始有明显改善,其中一位7岁的女孩甚至在第4个月便能脱离人工耳蜗,与母亲正常对话。年龄跨度大至22岁,但即使是14岁和23.9岁的青少年与成人,也表现出明显听力回升。更重要的是,在长达一年的随访中,无一人出现严重不良反应,常见副作用仅限于轻度血象波动,如中性粒细胞减少、血小板升高等。

此处也可插入视频替换上图
7岁的女孩与母亲正常对话(图片来源:参考文献[1])
研究人员对个体数据做了详细分析。比如23岁的成年女性,虽然血液中检测不到病毒拷贝,但体内的中和抗体水平提示她仍产生了免疫反应,并在六个月内将听力从101分贝改善至70 分贝。这意味着即使成年,疗法仍有希望生效。
而在另一个例子中,3岁的患儿在第一次注射后听力改善不理想,研究团队为其同一侧耳朵进行第二次注射,结果也观察到更进一步的恢复,表明多次给药在安全性上是可行的,也可能提升疗效。
总的来看,这项研究不仅验证了AAV-OTOF基因疗法在临床上的可行性,也首次将治疗范围从儿童扩展到了青少年与成人,为超过20万人带来了治愈希望。
而更深层次的价值在于,它不仅让听到成为可能,更意味着重新与世界建立联系。对这些患者而言,一次注射,不只是听力的回归,更是人生轨迹的重写。
总结
基因疗法,曾是遥不可及的未来医疗,如今正在悄然改写耳聋患者的命运。在这项由中国科研团队主导的临床试验中,研究人员用一次病毒载体注射,将健康的OTOF 基因送入患者耳蜗,使听觉重新上线。无论是年幼的孩子,还是二十多岁的成年人,几乎所有人都在一个月内开始听见世界。这是一次技术的突破,更是一场关于人类感知能力的修复。
尽管距离普及尚有距离,尽管个体差异仍在,副作用、价格、伦理也待解,但这项成果已足以让我们相信,某些遗传性耳聋正在从“终身缺陷”变成“可治疗病”。未来,我们或许可以为更多失声的孩子和家庭,打开一扇窗,让声音再次流入生命。
参考文献:
[1] Qi, Jieyu, et al. "AAV gene therapy for autosomal recessive deafness 9: a single-arm trial." Nature Medicine (2025): 1-10.
[2] Askew, Charles, et al. "Tmc gene therapy restores auditory function in deaf mice." Science translational medicine 7.295 (2015): 295ra108-295ra108.
[3] Roux, Isabelle, et al. "Otoferlin, defective in a human deafness form, is essential for exocytosis at the auditory ribbon synapse." Cell 127.2 (2006): 277-289.
[4] Lv, Jun, et al. "AAV1-hOTOF gene therapy for autosomal recessive deafness 9: a single-arm trial." The Lancet 403.10441 (2024): 2317-2325.
作者丨Denovo科普团队(赵丽丽 中国科学院大学博士;杨超 博士)
审核丨邵文亚博士 福建医科大学副教授
图文简介
