用LED灯治癌?科学家找到更温和的光热解决方案
近年来,癌症治疗虽不断取得进步,除手术治疗外,但化疗和放疗依旧是主流治疗手段。它们通过化学药物或高能辐射攻击癌细胞,却往往也损伤健康组织,使患者在治疗中承受强烈的身体负担和心理压力。科学界一直希望找到一种既能精准杀伤肿瘤,又能最大限度保护正常细胞的方法。
近期,有科学家提出了一项基于光的全新方案,用光来杀死癌细胞!相比昂贵、复杂的激光设备,这一方法使用低成本的LED光源,更安全、可扩展,也更接近临床实际应用的需求。这种光热疗法的出现,意味着癌症治疗正在从全身性攻击转向局部精准控制的新阶段,为未来更温和、更高效的治疗方式提供了新的可能。
光热疗法也能抗癌
光疗是一种利用特定波长光照射组织并诱导生物效应的治疗方式,已成为癌症研究中的重要方向。根据作用机制不同,光疗可分为三种主要类型,光动力疗法、光热疗法和光免疫疗法。其中,光热疗法通过光照激发光热材料,将光能转化为热能,从而使局部温度升高并破坏癌细胞结构。
光热疗法原理示意图(图片来源:参考文献[1])
在光热疗法中,如何找到对的材料至关重要,而材料的吸光能力与光源类型是影响疗效的关键因素。传统方法常使用高功率激光产生集中能量以加热肿瘤组织,但这种方式存在设备昂贵、操作复杂和热损伤风险等问题。
相比之下,近红外光特别是700至900纳米波段的光线,具有更强的组织穿透能力和更好的生物安全性。研究团队在此基础上使用了普通近红外LED光源,其光能分布更均匀、强度温和,不易灼伤周围健康组织,适合在体表或浅层组织进行治疗。
我们在上文提到过,光热疗法的原理在于利用光热剂材料吸收近红外光并产生局部升温。癌细胞对温度变化更为敏感,当局部温度升高至43至55摄氏度时,细胞膜结构被破坏,蛋白质变性,细胞逐渐失去活性。与药物化疗依赖化学反应不同,这一物理过程避免了毒副作用,也不会引发系统性损伤。更重要的是,光照范围可通过设备控制,热效应仅限于照射区域,使治疗更具选择性和安全性。
此外,光热疗法还能与其他治疗方式形成协同作用。局部升温可增加血流量与组织通透性,从而促进药物渗透,也能激活免疫反应,提高机体清除残余肿瘤细胞的能力
SnOx纳米片精准温和消灭癌细胞
在近期的研究中,德克萨斯大学奥斯汀分校科学家团队利用锡氧化物纳米片(SnOx nanoflakes)实现了更高效的光热转化和更强的癌细胞选择性杀伤能力。该材料由锡二硫化物(SnS₂)经过电化学氧化转化而成,厚度不足20纳米,呈片状结构,能够高效吸收810纳米近红外光并将其转化为热能。这种结构在光照下产生稳定而均匀的局部升温效果,是传统金属或碳基光热材料难以同时兼顾的性能。
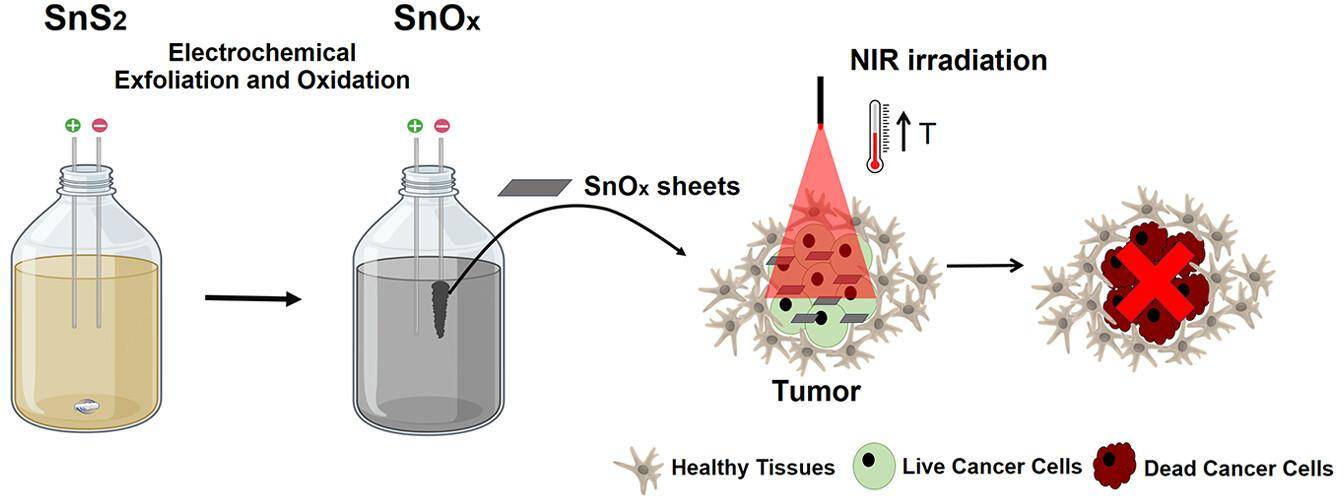
锡氧化物纳米片杀死癌细胞示意图(图片来源:参考文献[2])
研究表明,当SnOx纳米片在低强度LED照射下工作时,可以将93%的光能转化为热能。在体外实验中,30分钟照射即可使皮肤癌细胞死亡率达到92%,结直肠癌细胞死亡率约为50%,而对健康皮肤成纤维细胞没有显著影响。这种显著的选择性来自于癌细胞代谢较快、耐热能力较弱的特性,同时也与SnOx纳米片在细胞膜附近的分布有关,使热量能更集中地作用于肿瘤细胞区域。
总结
光热疗法的发展正让癌症治疗变得更加精准和温和。研究人员通过改进材料与光源,使治疗过程从依赖高功率激光的实验室操作,走向可以在临床甚至家庭中实现的可控治疗。锡氧化物纳米片的出现,为光热疗法提供了新的材料基础,它具备高效率、低毒性和可重复使用等优势。与低成本的近红外LED光源结合,这项技术展示了在安全性和可及性上的巨大潜力。
目前,这项研究仍处于实验阶段,但从技术路线和结果来看,它为未来癌症的辅助治疗提供了新的可能。通过精确控制局部温度、保护正常组织,同时实现高效杀伤肿瘤细胞,这类方法或将成为手术后预防复发的新选择。光热治疗的进步,不仅是材料科学的突破,也反映了医学向更人性化方向的发展。
参考文献:
[1] Cai, Yeyu, et al. "Phototherapy in cancer treatment: strategies and challenges." Signal Transduction and Targeted Therapy 10.1 (2025): 115.
[2] Chang, Hui-Ping, et al. "SnO x Nanoflakes as Enhanced Near-Infrared Photothermal Therapy Agents Synthesized from Electrochemically Oxidized SnS2 Powders." ACS nano 19.38 (2025): 33749-33763.
策划制作
作者丨杨 超 深圳理工大学科普主管、中国科普作家协会会员
审核丨赵宝锋 辽宁生命科学学会会员、研究员
图文简介
